电话:028-60361599
邮箱:1540372901@qq.com
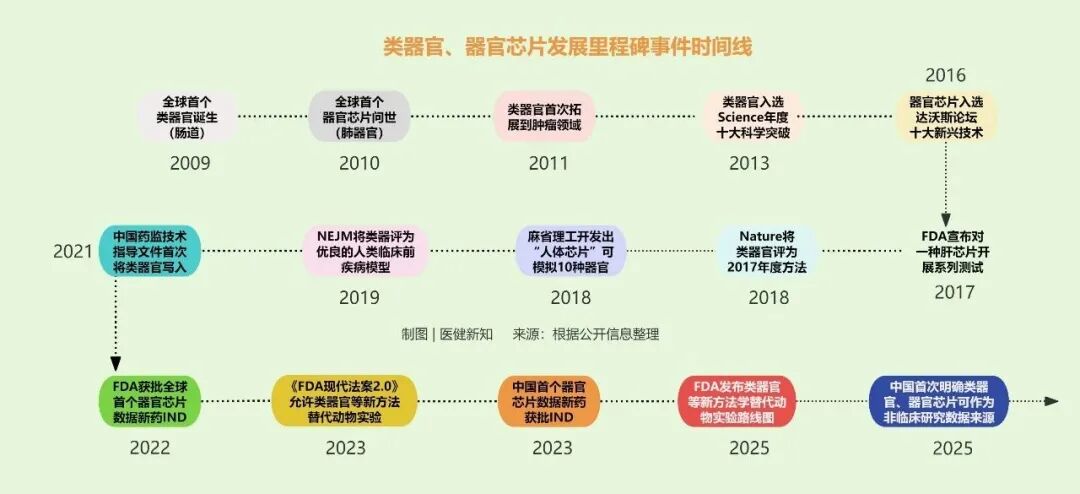
全球政策协同推进,行业范式转向在即
2026年初,全球生物医学研究领域迎来一系列标志性事件:荷兰发布国家技术战略行动议程,明确将器官芯片列为关键技术并规划十年2.6亿欧元投入;中国在国家自然科学基金中首次为“类器官与人工器官”设立独立申请代码C1004;美国、欧盟、英国等国也密集出台政策与资金计划,全力推动非动物模型在生物医学研究与药物开发中的应用。
一场以器官芯片和类器官为核心的生物医学研究范式转型,正在全球范围内加速展开。
荷兰:国家技术战略下的系统投资
荷兰发布《国家技术战略行动议程》,将器官芯片纳入生物分子与细胞技术重点方向,计划未来十年投入2.6亿欧元,围绕技术研发、标准化验证、规模化与国际推广展开系统布局,意味着器官芯片已从科研探索层面升级为国家战略性技术体系的一部分。
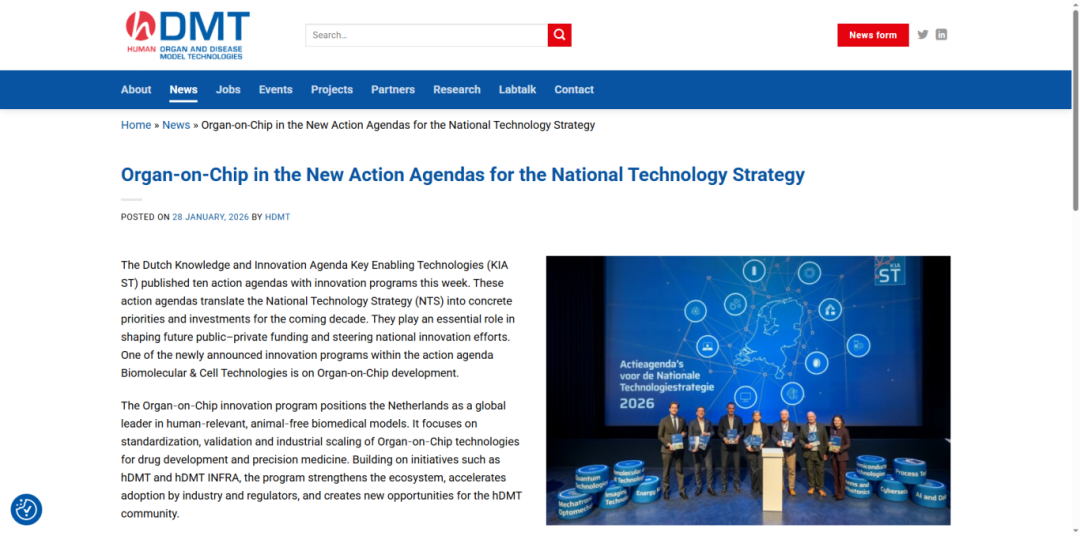
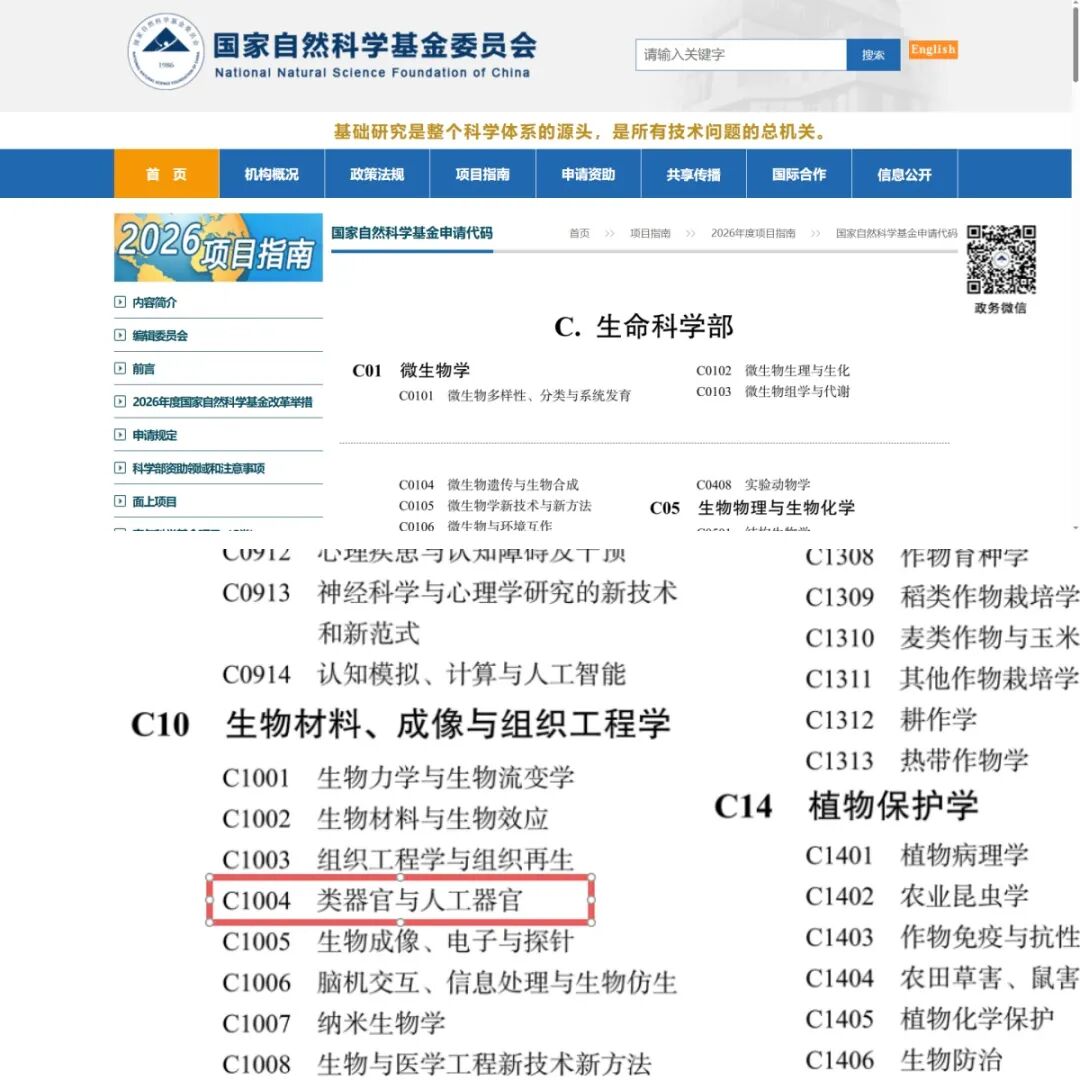
中国:类器官获独立国自然代码
2026年国家自然科学基金指南中新增“类器官与人工器官(C1004)”二级申请代码,标志着该领域在国内基础研究体系中正式获得独立地位。指南中明确支持高仿生疾病模型构建、血管—神经—免疫协同、标准化与自主设备研发,从源头创新到转化应用全链条布局。
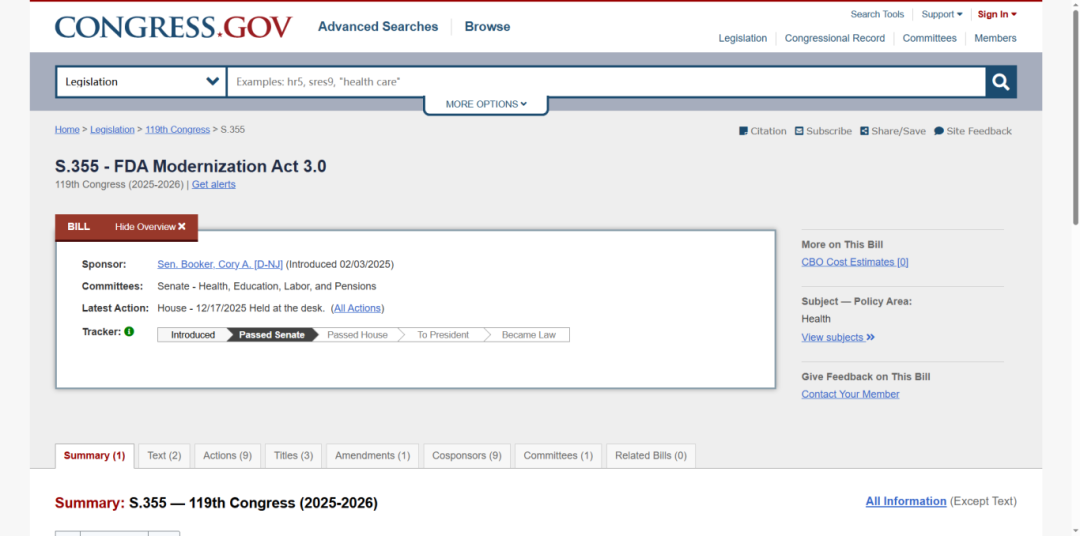
美国:立法、资金、监管三管齐下
美国通过《FDA现代化法案3.0》,赋予类器官等非动物方法与传统动物试验同等的监管地位。国立卫生研究院(NIH)也随之调整资助政策,明确要求新项目必须包含非动物研究方法,并专项推进类器官模型标准化,将其纳入新药申报与剂量设计的核心依据。
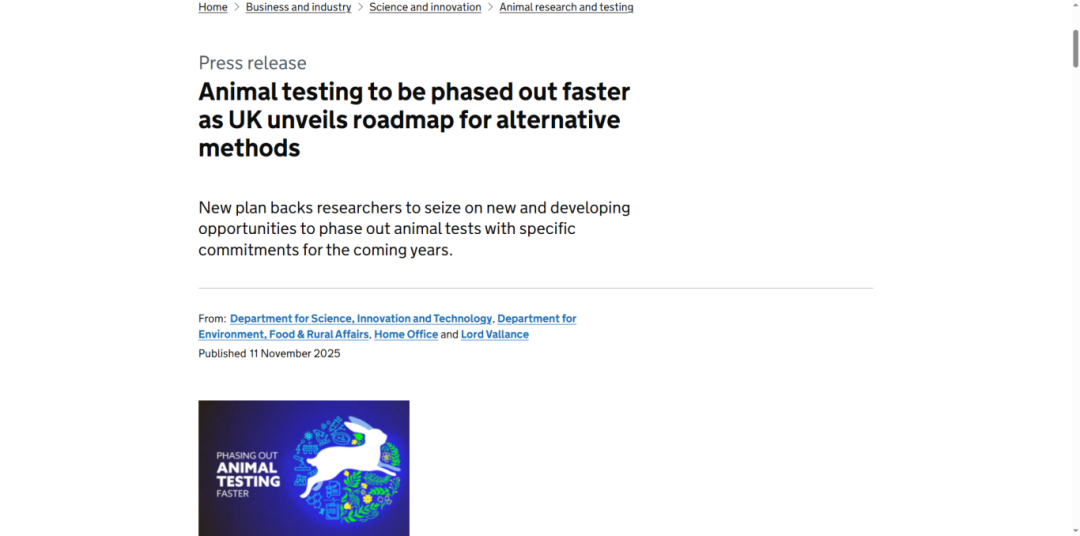
欧盟与英国:法律与路线并行
欧盟通过《欧洲化学工业行动计划》,2026年起逐步淘汰化学品安全评估中的动物实验,全面转向类器官等新方法;英国发布《动物实验替代技术路线图》,设定明确替代时间表,投入7590万英镑建立转化模型中心。
这些几乎同步的政策动向揭示了几个明确的全球趋势:
一、替代与减少动物实验已成为不可逆的行业共识,为类器官与器官芯片技术在药物研发、毒性测试等领域的应用打开了广阔空间。
二、技术的标准化与验证是当前阶段的关键挑战与焦点。无论是美国FDA的“替代方法工作组”,还是荷兰议程中强调的跨实验室可重复性,都致力于解决模型一致性、数据可靠性问题,以打通技术迈向监管认可和产业应用的“最后一公里”。
三、全链条布局成为共同特征。各国政策均涵盖了从基础研究、技术开发、平台建设到监管协调、市场培育的多个环节,旨在构建完整的创新生态。
在这一全球浪潮中,中国企业正从技术追随者向创新推动者转变。迪亚生物作为国内首家高通量器官芯片自动化解决方案平台企业,不仅实现了首台套重大技术装备的落地与验证,更依托与顶尖科研医疗机构合作,推动自主技术向药物研发、毒性评估等场景的规模化应用,如今在该领域已逐步建立起从政策支持、科研积累到产业转化的初步体系。

器官芯片与类器官,不再只是实验室里的微缩模型,更是全球生物医学创新体系中的关键节点。总结而言,全球政策协同、资金倾斜、技术快速迭代,标志着类器官与器官芯片已从“前沿探索”进入“系统布局”和“应用落地”的新阶段。在政策、资本与技术的三重驱动下,一个更高效、更精准、更人性化的生物医学研究新时代,正在我们眼前展开。
参考材料:
https://www.hdmt.technology/2026/01/28/organ-on-chip-in-the-new-action-agendas-for-the-national-technology-strategy/
https://www.nsfc.gov.cn/p1/2931/3971/4078/nrjj2026.html
https://www.congress.gov/bill/119th-congress/senate-bill/355
https://www.gov.uk/government/news/animal-testing-to-be-phased-out-faster-as-uk-unveils-roadmap-for-alternative-methods

